Neuer Therapieansatz bei HER2-positivem Brustkrebs entdeckt
Resistenzen gegen HER2-gerichtete Therapien sind häufig ein Problem zur Behandlung von Patientinnen mit HER2-positivem (HER2+) Brustkrebs. Daher ist die Identifizierung neuer Therapien für diese Patientengruppe wichtig.
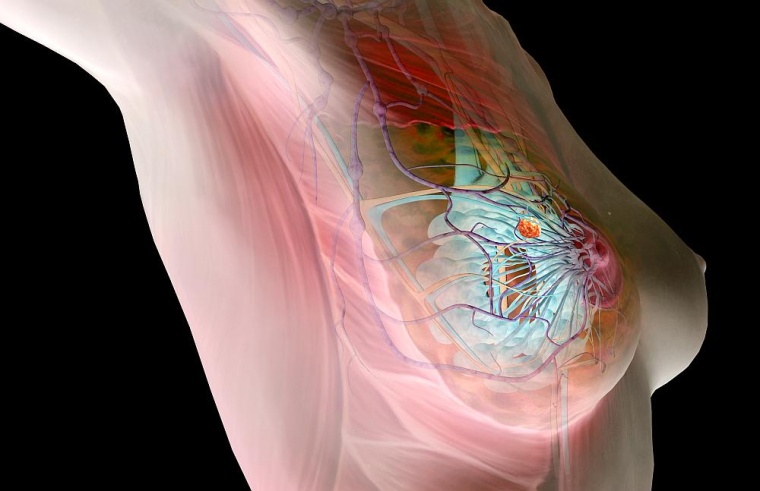
Forschende des Leibniz-Instituts für Arbeitsforschung an der TU Dortmund (IfADo) konnten bereits darstellen, dass das Enzym EDI3 mit Veränderungen im Stoffwechsel von Krebszellen in Verbindung steht. Ihre jetzt veröffentlichten Ergebnisse zeigen, dass die Hemmung von EDI3 ein neues therapeutisches Ziel bei Patientinnen mit therapieresistentem ER-HER2+ Brustkrebs sein kann.
Tumorzellen verändern ihren Stoffwechsel, um immer weiter wachsen zu können und so ihr Überleben zu sichern. Enzyme regulieren den Stoffwechsel und sind deshalb mögliche Ansatzpunkte für zielgerichtete Krebstherapien. Forschende am IfADo haben bereits ein solches Enzym – EDI3 –identifiziert. Die Glycerophosphodiesterase EDI3, die Glycerophosphocholin zu Cholin und Glycerin-3-phosphat spaltet, beeinflusst den Cholin- und Phospholipidstoffwechsel und wurde in vitro mit krebsrelevanten Eigenschaften in Verbindung gebracht. Während die Bedeutung des Cholinstoffwechsels bei Brustkrebs bereits untersucht wurde, ist die Rolle von EDI3 bei dieser Krebsart noch nicht erforscht worden.
Beeinflussung von EDI3 als therapeutischer Ansatz bei ER-HER2+ Brustkrebs
In einer aktuellen Studie konnten die Forschenden zeigen, dass die EDI3-Expression in ER-HER2+ Brusttumoren beim Menschen am höchsten ist und dass sowohl die Expression als auch die Aktivität in ER-HER2+ Brustkrebszelllinien am höchsten waren. Die Ausschaltung von HER2 sowie die Hemmung der HER2-Signalübertragung verringerten die EDI3-Expression. Die Hemmung von EDI3 verringerte wiederum vor allem die Lebensfähigkeit von ER-HER2+ Zellen. Darüber hinaus verringerte die Hemmung von EDI3 in ER-HER2+ Zellen, die gegen eine auf HER2 gerichtete Therapie resistent sind, die Zelllebensfähigkeit in vitro und das Tumorwachstum in vivo bei Mäusen.
Daraus schließen die Forschenden zum einen, dass EDI3 bei ER-HER2+ Brustkrebs im Vergleich zu anderen Subtypen hochreguliert ist. Zum anderen führt die Hemmung von EDI3 zu einer deutlichen Verringerung der Lebensfähigkeit und des Tumorwachstums, insbesondere bei Zellen, die gegen herkömmliche ER- HER2+ Therapien resistent sind. Die gezielte Beeinflussung von EDI3 kann also ein therapeutischer Ansatz sein, um die Wirkung von Standardtherapien zu verstärken, oder eine Alternative im Falle einer Resistenz gegen Standardtherapien.
Rezeptorstatus des Tumors
HER2 ist der Name eines Wachstumsfaktor-Rezeptors. Seine Aufgabe ist es, Signale von der Zelloberfläche aufzunehmen, ins Zellinnere zu leiten und damit die Zellteilung anzuregen. Liegt dieser Wachstumsfaktor-Rezeptor in zu großer Menge vor, spricht man von HER2+ – einem Subtyp von Brustkrebs. In Folge der vielen Wachstumssignale kann sich der Tumor unkontrolliert teilen. Es gibt Medikamente, die spezifisch auf HER2 abzielen. Die meisten Patientinnen sprechen erfolgreich darauf an, einige entwickeln jedoch Resistenzen. Deshalb sind alternative Behandlungsansätze notwendig.
Das Hormon Östrogen kann das Wachstum von Brustkrebszellen ebenfalls beeinflussen. Östrogen dockt an Bindungsstellen (Hormonrezeptoren) der Zelle an, die dann das Wachstumssignal ins Zellinnere weiterleiten. Um zu ermitteln, ob ein Tumor hormonabhängig wächst, wird untersucht, wie groß der Anteil der Zellen und die Menge der entsprechenden Hormonrezeptoren ist. Ausgedrückt wird das Ergebnis durch die Angabe ER+ (Östrogenrezeptor-positiv) oder ER- (Östrogenrezeptor-negativ).