Plötzlicher Herztod: 3D-Bildgebung zeigt mögliche Ursache
Ein Bildgebungsverfahren von Freiburger Forschern liefert Erkenntnisse zu Herzrhythmusstörungen, die den plötzlichen Herztod auslösen können.
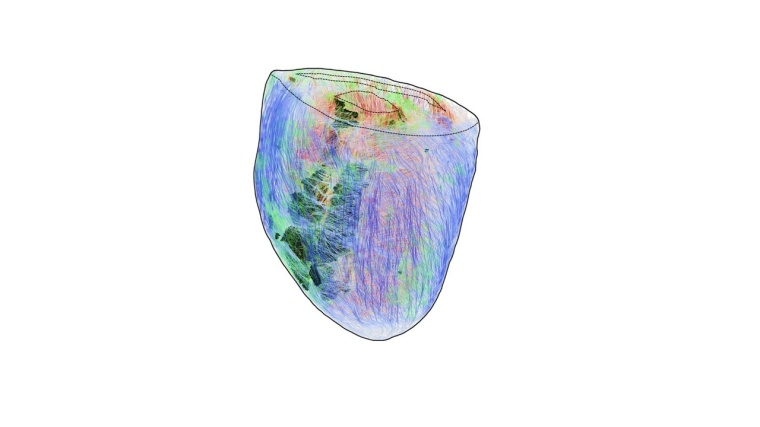

Die entdeckten Veränderungen könnten erklären, warum manchmal auch scheinbar gesunde Menschen betroffen sind. Die Ergebnisse wurden im Fachjournal Nature Cardiovascular Research veröffentlicht.
Freiburger Mediziner haben einen möglichen Grund gefunden, warum es bei vermeintlich gesunden jungen Menschen zum plötzlichen Herztod kommen kann. Mit einer neuen dreidimensionalen Bildgebungsmethode zeigten sie im Tiermodell: Narbengewebe im Herzen kann elektrische Signale auf eine Weise verändern, die in Ruhe unauffällig bleibt – aber bei Belastung zu gefährlichen Rhythmusstörungen führen kann. Gemeinsam mit Mitgliedern des italienischen Nationalen Forschungsrats konnten die Forscher*innen der Medizinischen Fakultät der Universität Freiburg diesen Mechanismus sichtbar machen. Die Ergebnisse wurden am 6. Oktober 2025 im Fachjournal Nature Cardiovascular Research veröffentlicht. Die Erkenntnisse könnten helfen, bislang unerklärte Fälle besser zu verstehen – und die Diagnostik bei Risikopatient*innen gezielter zu gestalten.
„Unsere Studie zeigt, dass Narbengewebe im Herzen nicht einfach stört – es beeinflusst aktiv, wie das Herz arbeitet“, sagt Prof. Dr. Peter Kohl, Direktor des Instituts für Experimentelle Kardiovaskuläre Medizin am Universitätsklinikum Freiburg. „Das hilft uns, die elektrischen Ursachen von Rhythmusstörungen besser zu verstehen – und langfristig auch, Diagnose und Behandlung gezielter zu gestalten.“
Wenn Narben das elektrische Herzsignal verändern
Im Zentrum der Untersuchung standen Mäuse mit einer genetisch bedingten Form der Herzmuskelerkrankung, wie sie auch beim Menschen auftritt – insbesondere bei jungen Patient*innen mit hohem Risiko für plötzlichen Herztod. Mithilfe einer neu entwickelten Kombination aus hochauflösender 3D-Bildgebung und optischen Messungen der elektrischen Erregung konnten die Forschenden zeigen: Narbengewebe, das bei solchen Erkrankungen entsteht, verändert die Ausbreitung elektrischer Signale im Herzen nicht pauschal, sondern abhängig von der Herzfrequenz. Bei normalem Herzschlag verliefen die elektrischen Impulse weitgehend ungehindert. Sobald das Herz jedoch schneller schlägt – etwa bei körperlicher Anstrengung oder emotionalem Stress – wurden die Signale durch das vernarbte Gewebe abgeschwächt oder blockiert.
Diese Wirkung ist vergleichbar mit einem technischen „Tiefpassfilter“: Schnelle Impulse werden gezielt gedämpft, langsamere bleiben unbeeinträchtigt. Dieser bislang unbekannte Mechanismus könnte erklären, warum Betroffene in Ruheuntersuchungen unauffällig erscheinen, obwohl bei Belastung ein hohes Risiko für gefährliche Rhythmusstörungen besteht.
Grundlage für digitale Zwillinge des Herzens
Ein weiteres zentrales Ergebnis der Studie: Allein die Struktur des Herzens reicht nicht aus, um das Risiko für Rhythmusstörungen zuverlässig vorherzusagen. „Wir brauchen digitale Modelle, die nicht nur die Anatomie, sondern auch die elektrischen Eigenschaften der verschiedenen Herzzellen berücksichtigen“, erklärt Dr. Francesco Giardini, Wissenschaftler am Institut für Experimentelle Kardiovaskuläre Medizin des Universitätsklinikums Freiburg. Genau dafür liefert die Studie wichtige Grundlagen. Ziel ist es, sogenannte digitale Zwillinge zu entwickeln – also individuelle Computermodelle, die für einzelne Patient*innen erstellt werden. Diese sollen es ermöglichen, Risiken besser einzuschätzen und gezielt zu behandeln, bevor es zu lebensbedrohlichen Ereignissen kommt.
Nächste Schritte: Weg zur klinischen Anwendung
Die aktuellen Ergebnisse beruhen auf einem etablierten Tiermodell, das wesentliche Merkmale der menschlichen Erkrankung abbildet. Eine wichtige Einschränkung ist jedoch, dass die Daten bisher nur im Mausmodell erhoben wurden. In einem nächsten Schritt sollen daher größere Tiermodelle untersucht werden, um die Übertragbarkeit auf den Menschen weiter zu prüfen.
Langfristiges Ziel ist es, die Bildgebungsverfahren so weiterzuentwickeln, dass sie klinisch nutzbar werden – etwa für individuelle Risikoabschätzungen oder zur Therapieplanung bei Patient*innen mit Herzmuskelerkrankungen und Narbengewebe. Die Forschungsarbeiten wurden im Rahmen des Sonderforschungsbereichs SFB1425 „The Heterocellular Nature of Cardiac Lesions“ an der Universität Freiburg gefördert. Für die Weiterentwicklung der Methode wurde kürzlich ein ERC Advanced Grant an Dr. Leonardo Sacconi, Seniorautor der Studie und Gastwissenschaftler am Institut für Experimentelle Kardiovaskuläre Medizin, vergeben.
Anbieter
Albert-Ludwigs-Universität Freiburg im BreisgauFahnenbergplatz
79085 Freiburg
Deutschland
Meist gelesen

Prof. Sven Meuth übernimmt die Klinik für Neurologie am UKM
Univ.-Prof. Sven Meuth hat zum 1. Februar die Leitung einer der größten Kliniken des UKM (Universitätsklinikum Münster) übernommen.

Helga-Reifert-Preis für Krebsforschung
Dr. Johannes Falter und Dr. Benedikt Wagner vom Universitätsklinikum Regensburg erhielten für ihre Krebsforschung den Helga-Reifert-Preis.

Wicker-Kliniken stellen neurologische Versorgung in Bad Zwesten und Bad Wildungen neu auf
Die Wicker-Kliniken stellen ihre neurologische Versorgung für die Zukunft auf: Im ersten Quartal 2026 wird der Krankenhausbereich der Hardtwaldklinik I in Bad Zwesten – mit neurologischer Akutklinik (Phase A), neurologischer Frührehabilitation (Phase B), MS-Ambulanz und Radiologie – an die Werner Wicker Klinik in Bad Wildungen verlagert. Der Rehabereich bleibt am Standort und wird ausgebaut.

Dr. Rolf Glazinski wird Chefarzt der Neurologie an der Wicker Klinik
Zum 1. Januar 2026 übernimmt Dr. Rolf Glazinski (61) die chefärztliche Leitung der Neurologie an der Wicker Klinik.

Neuer operativer Geschäftsführer und neue Pflegedirektion am Klinikum Frankfurt (Oder)
Das Klinikum Frankfurt (Oder) verstärkt seine Führungsspitze. Christopher Arndt (37) wird zum 1. März 2026 zum operativen Geschäftsführer des Klinikums Frankfurt (Oder) bestellt.