Zellen vollautomatisch kultivieren, selektieren und analysieren
11.04.2012 -
Zellkulturen sind das tägliche Arbeitsmaterial bei der Suche nach pharmazeutischen Wirkstoffen, Impfstoffen oder der Entschlüsselung von Genfunktionen. Die aufwendige Kultivierung wird auch heute noch vorwiegend von Hand durchgeführt. Fraunhofer IPM hat gemeinsam mit Partnern an einem vollautomatischen System zur Zellkultivierung gearbeitet. Ein automatisches Mikroskop, kombiniert mit intelligenter Software, sorgt für kontinuierliches Monitoring, eine optimale Steuerung und Dokumentation des Kulturprozesses.
Wissenschaftler der Fraunhofer-Institute IPM, IPA und FIT haben mit dem CellCultivator einen Zellkulturautomaten in Zusammenarbeit mit dem Max-Planck-Institut für Molekulare Zellbiologie und Genetik (MPI-CBG) entwickelt. Der CellCultivator erledigt die Routinearbeit der Zellkultivierung vollautomatisch und mit hohem Durchsatz - vom Einschleusen der Zellkulturen bis hin zur Auswertung der Ergebnisse. Die Automatisierung spart nicht nur wertvolle Zeit hoch qualifizierter Labormitarbeiter, sondern sorgt durch standardisierte Protokolle für höhere Effizienz und Reproduzierbarkeit der Prozesse.
An zentraler Stelle befindet sich ein Handling-Roboter, der die Kulturen in Mikrotiterplatten (von 6 Well bis 1.536 Well) zu den einzelnen Stationen transportiert. Die Verwendung von Standard-Kulturgefäßen oder von Zellkulturflaschen erleichtert den Übergang vom manuellen Betrieb in die automatische Kultivierung. Standardisierte Zellkulturbedingungen (37°C, bis zu 90% relativer Feuchte, 5% CO2-Gehalt) herrschen dort, wo die Kulturen sich über längere Zeit aufhalten, sodass auch Langzeituntersuchungen möglich sind. Das System besteht im Wesentlichen aus sechs flexiblen Modulen, die teilweise auch unabhängig voneinander nutzbar sind:
- Robotik zur automatischen Steuerung (Fraunhofer IPA)
- Liquid-Handling-Einheit (Fraunhofer IPA)
- automatisches Mikroskop mit Mustererkennungsfunktion (Fraunhofer IPM/FIT)
- Kolonie-Picker zur Selektion ausgewählter Zellareale (Fraunhofer IPA/IPM)
- Schleuse (Fraunhofer IPA)
- Lagerinkubator zur Aufbewahrung der Kulturen (Fraunhofer IPA)
Die Zellen im Blick: Monitoring mit automatischem Mikroskop
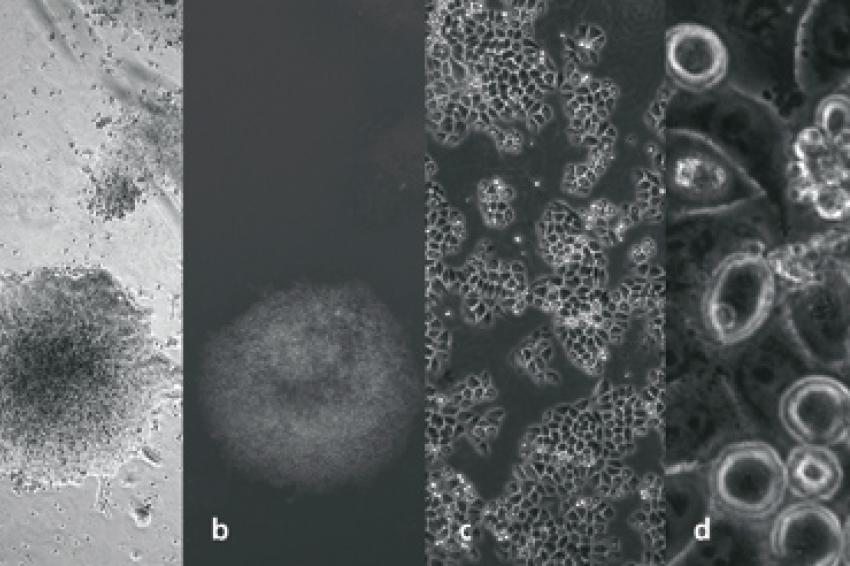
Ein am Fraunhofer IPM entwickeltes automatisches Mikroskop mit intelligenter Bildverarbeitung erfasst und dokumentiert den Zustand der Kulturen zu jedem Zeitpunkt des Prozesses. Aktuelle Messwerte wie z.B. Bedeckungsgrad, Fluoreszenzeigenschaften oder morphologische Eigenschaften der Zellen fließen in die Systemsteuerung ein. So optimiert das System die Abläufe automatisch und individuell für jede Kultur - eine bislang einzigartige Funktion in der automatisierten Zellkultivierung. Das inverse Mikroskop arbeitet dabei autonom: von der Überführung der Trägerplatten auf den Mikroskop-Tisch über die Fokussierung, den Objektivwechsel bis hin zur Ansteuerung der Lichtquellen. Das Optik-Modul ist speziell an die Zellkulturbedingungen, vor allem die hohe Feuchtigkeit, angepasst; alle relevanten optischen Komponenten sind gasdicht gekapselt.
Mustererkennung: Lernfähige Software optimiert Kulturprozess
Die zustandsabhängige Prozessierung der Kulturen wird durch die Kombination von mikroskopischer Optik und einer Mustererkennung möglich. Um die Muster der gewachsenen Zellen auf dem Trägermedium automatisch zu erkennen, wird die am Fraunhofer FIT entwickelte Software durch selbstlernende Algorithmen trainiert. Nachdem der Benutzer Beispielareale für Vordergrund und Hintergrund angegeben hat, werden Parameter wie zum Beispiel die Konfluenz oder die Anzahl fluoreszierender Zellen im Hochdurchsatz automatisch ermittelt. Die Lernfähigkeit der Software erlaubt eine Übertragung der Abläufe auf verschiedene Zelltypen.
Präzises Kolonie-Picking mit integrierter Abbildung
Beim Kolonie-Picking werden geeignete Areale einer Zellkultur ausgewählt und von einem Labormitarbeiter mit einer Pipette in ein neues Gefäß umgesetzt - alle übrigen Zellen werden verworfen. Die automatische Picking-Einheit besteht aus einem Picking-Arm inklusive Hohlnadel und einem am Fraunhofer IPM optimierten Mikroskop mit einer 5-fach-Vergrößerung, das mit Phasenkontrast im Durchlicht betrieben wird. Die zu entnehmenden Zellareale werden in der Optik-Einheit festgelegt, die Positionen übertragen und im Picker wiedergefunden. Die Bildaufnahme in der Picking-Einheit sorgt für eine Optimierung der Picking-Position und eine Bewertung des Picking-Ergebnisses - mit einer Genauigkeit im Mikrometerbereich.
Entschlüsselung der Gen-Funktion
Das MPI-CBG nutzt das System zur Entschlüsselung von Genfunktionen embryonaler Mausstammzellen: Über die Transfektion von Zellkulturen, also das Einbringen von Fremd-DNA, können ganze Genome untersucht, Proteine lokalisiert und deren Funktion bestimmt werden. Während der Kultivierung führt das System eine Bestimmung des Bedeckungsgrades durch. Oberhalb eines Schwellwertes wird eine Passage, d. h. eine Umsetzung in Subkulturen, eingeleitet, und die Zellen werden weiter expandiert. Um zu ermitteln, ob und wo genau die eingeschleusten Gene in der Zelle aktiv sind, bestimmt das System die Fluoreszenz von grün fluoreszierendem Protein (GFP), das als Marker von den Zellen produziert wird, und überprüft auf diese Weise die Transfektion.
Falls notwendig, werden mit dem Kolonie-Picker die relevanten Kolonien für die weitere Kultivierung ausgewählt. Vor dem Ausschleusen der Kulturen nimmt das Mikroskop Fluoreszenzbilder mit hoher Vergrößerung auf, um die Lokalisation der produzierten Proteine innerhalb der Zelle zu dokumentieren. Abschließend werden die Zellen außerhalb des Systems eingefroren. 500 Zellpools pro Monat generiert und analysiert der Zellkulturautomat. Der gesamte Prozess umfasst einen Zeitraum von circa zehn Tagen - ohne dass ein Labormitarbeiter Hand an die Kulturen legen muss.
Projektpartner sind das Fraunhofer-Institut für Angewandte Informationstechnik FIT, das Fraunhofer-Institut für Physikalische Messtechnik IPM, das Fraunhofer-Institut für Produktionstechnik und Automatisierung IPA und das Max-Planck-Institut für Molekulare Zellbiologie und Genetik MPI-CBG.
Kontakt
Fraunhofer Institut für Photonische Mikrosysteme IPMS
Maria-Reiche-Str. 2
01109 Dresden
Deutschland
+49 3 51 88 23-0
+49 3 51 88 23-266