IGRT: Neue Möglichkeiten in der bildgesteuerten Strahlentherapie
01.03.2013 -
IGRT: Neue Möglichkeiten in der bildgesteuerten Strahlentherapie. Das Ziel der modernen fraktionierten Strahlentherapie ist die Verabreichung hoher Bestrahlungsdosen in einer bestimmten Körperregion nach einer operativen Therapie bzw. auf einen noch vorhandenen Tumor.
Voraussetzung für die präzise Durchführung entsprechend der Planung sind eine Immobilisierung und eine korrekte Positionierung der Patienten, so dass die aus mehreren Raumrichtungen auf die Patienten gerichtete Strahlung den Körper präzise dort erreicht, wo sie es soll.
Wesentlich ist dabei die Positionierung des sog. Behandlungs-Isozentrums (Punkt, in dem sich alle Strahlen treffen). Je präziser dieser Vorgang, desto geringer kann der „Sicherheitsabstand“ um das Zielvolumen gewählt werden, der einerseits Positionierungsunsicherheiten kompensiert, andererseits aber mit zunehmender Größe das Auftreten von Nebenwirkungen begünstigt.
Für den Kopfbereich stehen seit langem verschiedene Positionierungssysteme zur Verfügung.
Die Positionierung im Körperbereich war bisher problematischer, was die Einführung von Präzisionsverfahren (z.B. extrakranielle stereotaktische Bestrahlung, intensitätsmodulierte Strahlentherapie, IMRT) erschwerte.
Während die Zielvolumendefinition seit Einführung der CT und MRT selbstverständlich bildgestützt ist, wird neuerdings die bildgestützte Patientenpositionierung zunehmend unter dem Paradigma „IGRT“ (Image Guided Radiotherapy, Bildgestützte Strahlentherapie) zusammengefasst.
Entsprechend ihrer Lokalisation bewegen sich die meisten Tumoren innerhalb des Körpers.
Die Position der Prostata-Tumoren ist abhängig von der aktuellen Blasen- und Rektumfüllung; Tumoren der Lunge und Leber bewegen sich synchron zu den Atemexkursionen. Die zur Kompensation dieser Beweglichkeit notwendige Vergrößerung des Zielvolumens resultiert in Erhöhung der Toxizität in den gesunden Geweben, während bei zu kleinen Zielvolumina Unterdosierungen der Tumorregion drohen.
Reduktion der Beweglichkeit des Zielvolumens durch Atemexkursionen kann invasiv durch Narkose unter Verwendung einer minimalen Beatmungsamplitude oder Tumor- Immobilisierung während des Atemzyklus unter apparativer Kontrolle („Active Breathing Control“) erreicht werden.
Entspannte, flache Atmung oder Atemanhaltemanöver ohne apparative Unterstützung („passive deep inspiratory breath hold“) werden am häufigsten verwendet.
Bemühungen konzentrieren sich darüber hinaus auf „gating“ (der Strahl wird nur bei optimaler Tumorposition eingeschaltet) oder „real-time target tracking“ (dauernde Anpassung der Bestrahlungsfelder an die Tumorposition).
Nachdem die Patientengeometrie immobilisiert ist, wird eine schnelle und präzise Lokalisation notwendig, um die korrekte Position des Isozentrums festzulegen. Die relativen Positionen von Isozentrum und Zielvolumen sollen während Planung und Behandlung übereinstimmen.
Therapiesimulatoren (Durchleuchtungs-/ Röntgenanlagen mit der Geometrie von Bestrahlungsgeräten) ermöglichten eine zweidimensionale Bildsteuerung. Die Lage des Isozentrums in Bezug auf die Oberflächen- und knöcherne Anatomie kann durch orthogonale Röntgenbilder festgelegt werden, die Bestrahlungsfelder können in Bezug auf die knöchernen Strukturen dokumentiert werden.
Die Feldposition am Beschleuniger kann durch mit dem Therapiestrahl angefertigte planare Aufnahmen mit Film/Kassettenkombinationen, sog. Feldkontrollen/ Portfilmen (nach Vergleichen mit Simulationsaufnahmen) überprüft werden. Bei einem Unterschied zwischen der Soll- und Ist-Position kann dies vor der Bestrahlung korrigiert werden.
Jedoch ist das System wegen mehrmaligen Anfertigen von Röntgenbildern zeit- und arbeitsaufwändig.
Eine filmlose Anfertigung von Aufnahmen mit dem Therapiestrahl stellt das sog. elektronische Portal Imaging mittels Röntgen/Halbleiterdetektoren dar. Dies kann beliebig oft wiederholt werden und liefert qualitativ hochwertige Aufnahmen.
Dynamische Sequenzen mehrerer Aufnahmen in kurzer Folge, also eine Art Film, kann auch während der Bestrahlung aufgenommen werden.
Röntgenbasierte automatisierte Positionierungs- und Verifikations- Systeme mit Infrarot Positionierund Trackingsystemen sind integriert in das Beschleunigersystem oder auch als alleinstehende Systeme verfügbar.
So kann die Bestrahlung – automatisiert und von außerhalb des Bestrahlungsraums – durch die Position eines im Körper gelegenen Targets getriggert werden, und Patientenbewegungen können während der Therapie detektiert werden.
Die für bestimmte Funktionalitäten solcher Systeme verwendeten Marker (sog. „Fiducials“, typischerweise aufgrund der Röntgendichte und der inerten Eigenschaften aus Gold) sind mit Röntgenmethoden detektierbar und stellen für die 2DVerfahren die einzige Möglichkeit dar, weichteilbezogen zu lokalisieren und ein „beam-gating“ durchzuführen.
Eine Alternative für die nonivasive und präzise 3D-Visualisierung von extrakraniellen Zielvolumina ist die Ultraschall-basierte Positionierung. Ein armgeführter Schallkopf wird räumlich in Bezug auf das Beschleunigerisozentrum kalibriert. Dann werden in Echtzeit die aus dem Bestrahlungsplanungssystem importierten Organstrukturen in ihrer Sollposition auf das Ultraschallbild überlagert.
Nach manuellem Matching wird dann ein Verschiebevektor errechnet und unter Kontrolle des Systems wird die Positionskorrektur durchgeführt. Der zeitliche Aufwand beträgt etwa 5 min/Patient/Tag.
Eine weitere Möglichkeit, Weichteil- Zielvolumina schnell 3D vor der Bestrahlung darzustellen, ist das „inroom“ CT, also eine CT-Bildgebung im Bestrahlungsraum in Bestrahlungsposition. Prinzipiell gibt es zwei große Gruppen von in-room CTs:
1. Standard-CT-Geräte, die in einer definierten geometrischen Beziehung mit dem Behandlungstisch/ dem Bestrahlungsgerät stehen.
2. an der Gantry montierte Cone-Beam CT-Systeme, die entweder mit einer zusätzlichen diagnostischen (kV) Röntgenquelle arbeiten und orthogonal zum Therapiestrahl orientiert sind oder die direkt den therapeutischen Strahl nutzen (MV).
Beide sind in der Lage, 3D-Darstellungen des Behandlungsvolumens unmittelbar vor der Bestrahlung anzufertigen. Die kV-Einheiten bieten prinzipbedingt (besserer Weichteilkontrast als MV) eher die aus der Diagnostik gewohnten Auflösungsund Kontrastverhältnisse.
Das Linac-adaptierte Cone-Beam CT (Elekta Synergy) ermöglicht die Herstellung von 3D-Abbildungen in der Bestrahlungsposition innerhalb einer Minute während einer 360° Gantry Rotation.
Die gewonnenen Radiographien können mit einem Algorithmus in einen Volumendatensatz konvertiert werden, der eine recht gute Auflösung von Weichteilgewebe bietet.
Dieser Volumendatensatz kann dann – automatisch oder manuell – mit dem Bestrahlungsplanungs- CT zur Deckung gebracht werden. In Kombination mit Hochpräzisionsbehandlungstischen mit sechs Freiheitsgraden kann die Patientenposition dann sofort translational oder auch bezüglich Rotationsfehlern korrigiert werden.
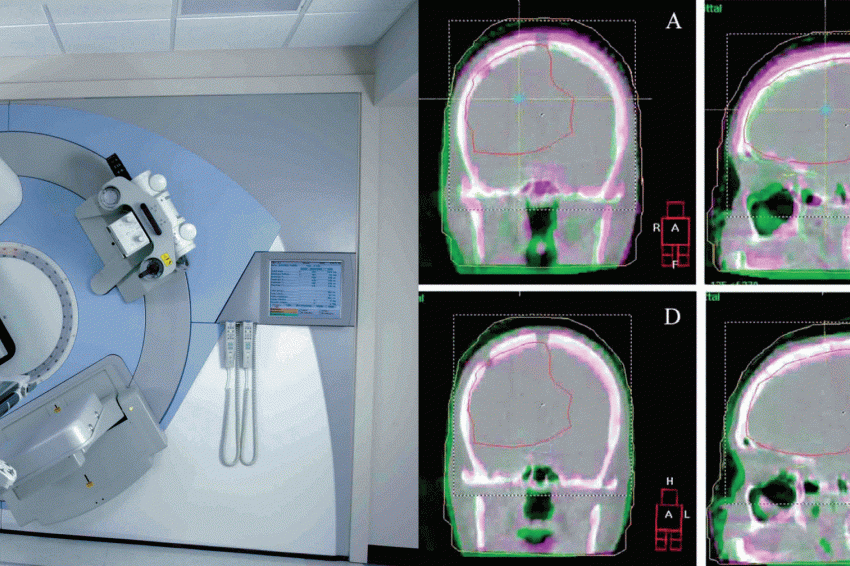
Abbildung 2 zeigt ein Positionskontrolle- und Korrektur vor einer Patientenbestrahlung im Schädelbereich. Zusätzlich kann auch dieses System im Fluoroskopie-Modus betrieben werden, so dass zusammen mit der MV-Einheit simultan orthogonale planare Aufnahmen angefertigt werden bzw. Filmsequenzen während der Bestrahlung akquiriert werden können.
Die Vorteile dieser Methode sind also die Schnelligkeit, die 3DDarstellung von Weichteilstrukturen, der Verzicht auf implantierte Marker und die minimale zusätzliche Dosisbelastung.
Das Ziel in der Zukunft ist die weitere Verbesserung der Bildqualität, die Beschleunigung der Bildakquisition und die Reduktion der Dosisbelastung während der Verifikation und damit die Ermöglichung von täglichen Kontrollen.
Kontakte:
Judit Boda-Heggemann
Frank Lohr
Frederik Wenz
Universitätsklinikum Mannheim
Klinik für Strahlentherapie und Radioonkologie
D-Mannheim
Tel.: 0621/383-3530
Fax: 0621/383-3493
judit.boda-heggemann@radonk.ma.
uni-heidelberg.de
frederik.wenz@radonk.ma.uni-heidelberg.de
www.uni-heidelberg.de