Orale Mukositis verliert an Schrecken
13.03.2013 -
Orale Mukositis verliert an Schrecken. Palifermin (Kepivance) hat die EU-weite Zulassung erhalten und steht jetzt auch in Deutschland zur Verfügung.
Der Keratinozyten- Wachstumsfaktor kann deutlich Schweregrad, Häufigkeit und Dauer einer Chemo- oder Strahlentherapie- bedingten oralen Mukositis reduzieren.
Zum Einsatz soll er vor allem bei Patienten mit hämatologischen Krebsarten kommen, insbesondere wenn sie myeloablative Therapien erhalten.
Die Problematik der oralen Mukositis beschrieb Prof. Dr. Dietger Niederwieser, Leipzig. „Die orale Mukositis wird von den Patienten als eine ungeheure Belastung empfunden“, sagte er.
Man muss derzeit in der EU von allein jährlich etwa 13.000 Krebspatienten ausgehen, die sich einer Transplantation peripherer Blutstammzellen unterziehen müssen, in Deutschland schätzt man die Zahl auf 4.500 Patienten. Alle sind Kandidaten für die orale Mukositis.
Dabei erläuterte Prof. Monika Engelhardt, Freiburg, anlässlich der Pressekonferenz von Amgen in Hamburg die Mukositis als ein Krankheitsbild, das im gesamten gastrointestinalen Trakt auftreten kann.
Dort kann es Ursache von Erythemen, Schwellungen, Blutungen und schmerzhaften Ulzerationen sein. Meist wird die orale Mukositis, die man meist auch als Stomatitis bezeichnet, durch eine Hochdosis- Chemotherapie oder Radiotherapie ausgelöst.
So leiden 70–80% der Patienten, die eine Transplantation mit hämatopoetischen Stammzellen erhalten, an einer solchen oralen Mukositis während ihrer Behandlungszeit.
Unangenehm für die Patienten ist noch das gestörte Geschmacksempfinden. Mögliche Komplikationen sind Infektionen – erläuterte Engelhardt – die das Risiko steigern, dass der Patient schließlich daran sterben muss.
Kausales Management der Mukositis
Nun ist ein Präparat auf dem Markt, das die orale Mukositis kausal therapierbar macht. Während die orale Mukositis in fünf verschiedenen Phasen abläuft, kann Palifermin als ein rekombinanter humaner Keratinozyten- Wachstumsfaktor diese beeinflussen.
Er besteht aus 140 Aminosäuren und weist einen Unterschied zum endogenen humanen Keratinozyten-Wachstumsfaktor auf: Es fehlt eine der ersten 23 Nterminalen Aminosäuren.
Schon in präklinischen Studien unterstützte Kepivance die Reparaturfunktionen der Zellen im Gastrointestinaltrakt. Es wirkt also stimulierend auf die Mukosa, regt das Wachstum der Epithelzellen an und schützt sie so vor Schäden durch Chemo- oder Radiotherapie.
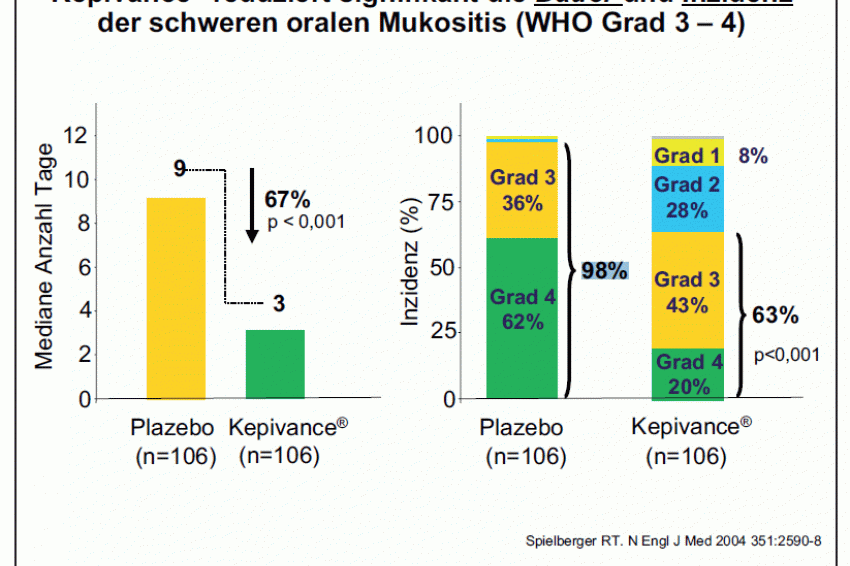
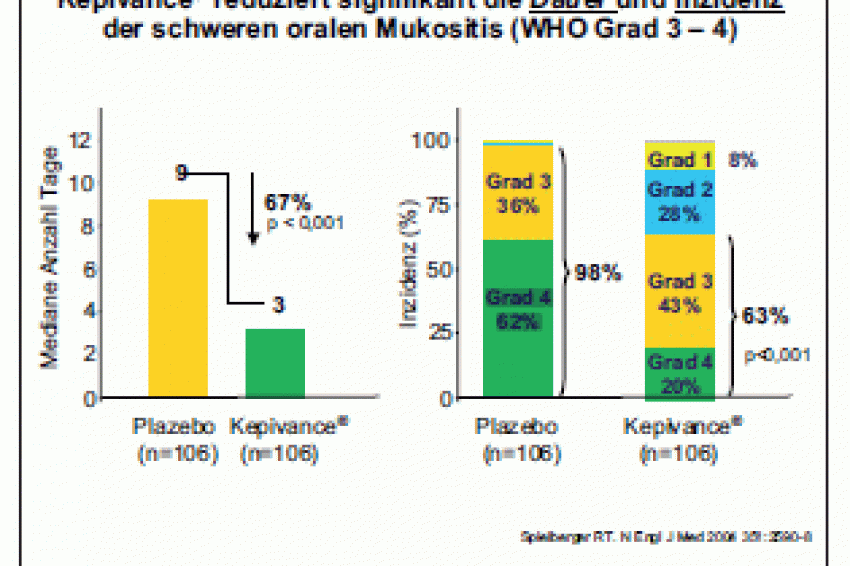
Zudem kann Palifermin signifikant Dauer und Inzidenz der schweren oralen Mukositis von WHO-Grad 3–4 um 67 % reduzieren (Abb. 1).
Studienergebnisse überzeugend
Mittlerweile gibt es vier klinische Studien (drei randomisierte, placebokontrollierte Untersuchungen und eine Studie zur Pharmakokinetik).
Insgesamt wurden hier 650 Patienten mit hämatologischen Krebsentitäten eingeschlossen.
In der randomisierten doppelblinden Phase- III-Studie, die Engelhardt erläuterte, bekamen 212 Patienten mit Leukämien oder Lymphomen entweder Placebo oder Palifermin.
Zur Krebstherapie erhielten sie eine myelotoxische Hochdosistherapie mit Etoposid und Cyclophosphamid sowie eine Ganzkörperbestrahlung, gefolgt von der Transplantation peripherer Blutstammzellen.
63 % der Patienten in der Palifermin-Gruppe und 98 % der Placebogruppe entwickelten eine Mukositis Grad 3 oder 4, die im Median drei bzw. neun Tage anhielt.
Die Häufigkeit von Grad- 4-Mukositiden ging mit Palifermin signifikant zurück (20 versus 62 %), ebenso der Verbrauch von Opioid- Analgetika.
Eine totale parenterale Ernährung war bei 31 % der Patienten gegenüber 55 % in der Placebogruppe notwendig.
Die Inzidenz der febrilen Neutropenie lag für Palifermin bei 75 % und konnte um 18% dadurch gesenkt werden, für Placebo lag sie bei 92 %.
Die häufigsten Nebenwirkungen waren Hautausschlag, Juckreiz, Erytheme, Beschwerden an Mund und Zunge sowie Geschmacksveränderungen, die aber meist mild bis moderat und vor allem reversibel waren.
Die meisten dieser Ereignisse (Rash, Pruritus, Schwellungen von Mund und Rachen und Geschmacksirritationen) entsprachen der pharmakologischen Wirkung von Kepivance auf das orale Epithel und die Haut.
Patienten, die das neu zugelassene Präparat erhielten, wiesen signifikant bessere Ergebnisse in den Fragebögen für den „Functional Assessment of Cancer Therapy“ im Hinblick auf physische und funktionale Lebensqualität auf.
Zwar blieb die Referentin Engelhardt noch zurückhaltend mit der Anmerkung, dass Palifermin bislang in den Studien keinen negativen Einfluss auf den Behandlungserfolg einschließlich Überleben hat.
Doch Prof. Niederwieser äußerte hoffnungsvoll, dass prospektive Studien in naher Zukunft zeigen könnten, dass sich Palifermin nicht nur besonders positiv auf die Lebensqualität der Patienten auswirkt, sondern sogar auch auf das Gesamtüberleben.
Pegfilgrastim – einmalig
Filgrastim (Neupogen) ist seit etwa 15 Jahren in Deutschland im Handel und hat sich zur Behandlung der Zytostatika-induzierten Neutropenie bewährt, berichtete Dr. Richard Schlenk, Ulm, über ein weiteres Präparat der Firma Amgen.
Filgrastim ist ein gentechnologisch produzierter Granulozyten-Kolonie-stimulierender Faktor (G-CSF), der nach subkutaner Verabreichung einen ausgeprägten Anstieg der neutrophilen Granulozyten im peripheren Blut bewirkt, dadurch vor Infektionen schützt und in vielen Fällen die Notwendigkeit einer Antibiotikatherapie reduziert.
Innerhalb von 24 Stunden steigt die Anzahl neutrophiler Granulozyten im peripheren Blut an; Monozyten und Lymphozyten reagieren kaum. Doch ein Nachteil des Proteins ist in der raschen Elimination zu sehen, wodurch bisher eine tägliche Injektion des Präparates notwendig war.
Die Pegylierung, also die Verknüpfung des Moleküls mit Polyethylenglykol, kann die Verweildauer von Proteinen im Organismus deutlich verlängern.
Seit 2002 steht Filgrastim deshalb auch in pegylierter Form zur Verfügung (Neulasta).
Aufgrund der längeren Halbwertzeit ist nur noch jeweils eine Injektion von 6 mg Wirkstoff in einem Chemotherapiezyklus – ca. 24 Stunden nach Zytostatikagabe – notwendig, um eine Neutropenie bzw. schwerwiegende Infektion zu verhindern.
Doch es gibt keine Unterschiede in der Wirksamkeit.
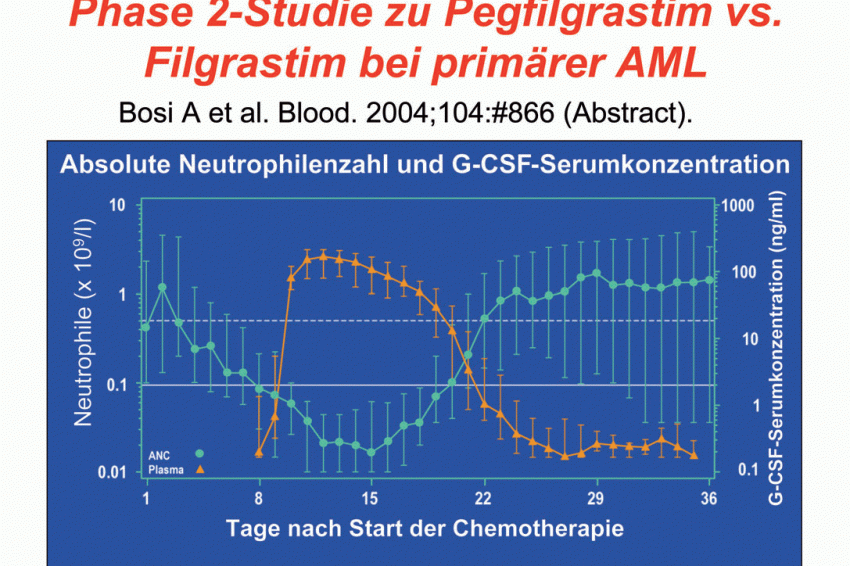
So ist in einer multizentrischen, doppelblinden, randomisierten Phase-II-Studie bei 84 Patienten mit einer de novo AML die Gabe einer Fixdosis Neulasta im Induktionszyklus 1 in Bezug auf die Reduktion der Dauer schwerer Neutropenie ebenso wirksam wie die Gabe von 16 Spritzen (im Median) Filgrastim – bei vergleichbarer Sicherheit und Verträglichkeit (Abb. 2).
Weiterhin wurde in einer umfangreichen Phase-III-Studie an Patientinnen mit Brustkrebs gezeigt, erläuterte Schlenk, dass fieberhafte Neutropenien nach einmaliger Gabe von Pegfilgrastim sogar seltener auftraten und verkürzt waren im direkten Vergleich zu einer mehrfachen Behandlung mit dem unveränderten GCS-F. Die Verträglichkeit beider Therapeutika war gleich, so Schlenk.
Die häufigsten unerwünschten Wirkungen waren Knochenschmerzen.
Moleküle unterschiedlich
Dabei unterscheiden sich die Moleküle Filgrastim und Pegfilgrastim vor allem in ihrer Kinetik, denn die Pegylierung vergrößert das Molekül stark.
Die Eliminiationshalbwertszeit des PEG-Proteins ist nahezu verzehnfacht, die Zeit bis zum Erreichen der maximalen Plasmakonzentration rund neunmal länger.
Es wird nicht über die Nieren ausgeschieden, sondern kann nur nach Bindung an den G-CSF-Rezeptor auf den Granulozyten abgebaut werden.
In zwei weiteren randomisierten Doppelblindstudien mit Patienten, die zusätzlich zu Doxorubicin und Docetaxel entweder Filgrastim oder Pegfilgrastim erhielten, waren beide G-CSF-Präparate vergleichbar gut wirksam und verträglich.
Sie reduzierten die Dauer einer schweren Neutropenie auf 1,6 bis 1,8 Tage. Ohne die Gabe ist bei diesem Therapieschema mit 5- bis 7-tägiger Neutropenie zu rechnen.
Über die gesamte Studiendauer lag die Rate der Patienten, die an neutropenischem Fieber litten, unter Pegfilgrastim tendenziell niedriger als unter Filgrastim (13 versus 20 % sowie 9 versus 18 %).
Dr. Nana Mosler, Leipzig