Kleines Zeichen, großer Nutzen
Warum sind CE-gekennzeichnete Medizinprodukte wichtig für den Klinikalltag?
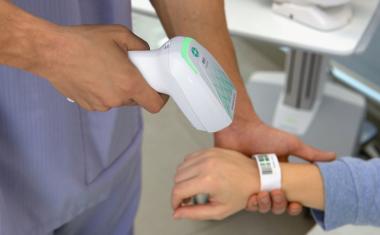
Jeder, der im klinischen Umfeld arbeitet, kennt das CE-Zeichen, das sichtbar an vielen Produkten wie Masken, Handschuhen, Spritzen oder Beatmungsgeräten angebracht ist. Das Zeichen steht für eine Vielzahl von regulatorischen Anforderungen, die Hersteller solcher Produkte einzuhalten haben.
Vor über 25 Jahren, am 1. Januar 1995, trat das Medizinproduktegesetz in Kraft. Damit war eine breite Grundlage geschaffen, die die Sicherheit der Anwendung von Produkten im Klinikalltag wesentlich erhöht hat. Am 25. Mai dieses Jahres läuft die Frist zur Umstellung auf die neue Medizinprodukteverordnung (MDR) für Medizinprodukte der Klasse I ab.
Verschärfung gesetzlicher Grundlagen
Damit verschärft sich die gesetzliche Grundlage für die Hersteller von Medizinprodukten. Neben der Einführung einer internationalen Kodierung (UDI-Code), die eine eindeutige Zuordnung der Produkte erlaubt, spielt die umfangreichere Verantwortlichkeit des Herstellers für den gesamten Produktlebenszyklus (Post Market Surveillance) eine große Rolle.
Die Firmen sind nunmehr aufgefordert nachzuweisen und zu dokumentieren, dass ihre Produkte auch innerhalb der ausgelobten Anwendungsdauer einwandfrei funktionieren. Auch unangekündigte Inspektionen, wie man sie bisher nur aus den USA kannte, gehören zur Neuerung der gesetzlichen Grundlage. Gerade in der jetzigen Situation kommt Produkten, die der Infektionsprävention dienen und somit der Medizinprodukteverordnung unterliegen, eine besondere Bedeutung zu. Endständige Sterilfilter mit einer eindeutigen Zweckbestimmung zur Infektionsprävention gehören dazu.
Vielzahl an hohen Anforderungen
Hersteller, die ihre Produkte in diesem Bereich mit einem CE-Zeichen versehen und als Medizinprodukte kennzeichnen, haben eine Vielzahl von Anforderungen zu erfüllen. Hierzu zählen:
- Risikoanalysen und -bewertungen;
- Klinische Untersuchungen und Nachweise der Evidenz;
- Technische Dokumentationen und Life-Cycle-Management;
- Verifizierungen und Validierungen aller Herstellungs- und Vertriebsprozesse;
- Rückverfolgbarkeit und Produkthaftung;
- Ein umfassendes, zertifiziertes Qualitätsmanagementsystem;
- Eine Biokompatibilitätsprüfung zum Schutz des Patienten.
So muss ein Hersteller von Medizinprodukten im ersten Schritt in Form eines Konformitätsbewertungsverfahrens überprüfen, ob das Produkt der Definition eines Medizinproduktes entspricht und die Bestimmung einen medizinischen Zweck erfüllt. Hersteller von endständigen Sterilfiltern können diese als Medizinprodukt kennzeichnen, wenn die Zweckbestimmung die Infektionsprävention beinhaltet.
Zweckbestimmung steht im Mittelpunkt
Im zweiten Schritt müssen klinische Studien und klinische Bewertungen den Nutzen des Produktes beweisen und zeigen, dass die Zweckbestimmung erfüllt wird. Gibt es bisher keine klinischen Beweise, die zeigen, dass das Produkt einen medizinischen Nutzen hat, kann auch keine Konformität ausgesprochen werden. Endständige Sterilwasserfilter sorgen evident für eine Infektionsprävention. Dies ist in zahlreichen veröffentlichten Studien nachgewiesen.
Beweist die klinische Bewertung den Nutzen des Produktes, ist zu überprüfen, ob das Qualitätsmanagementsystem des Herstellers auf Basis jährlicher Audits durch eine akkreditierte Prüfstelle zertifiziert ist. Das Qualitätsmanagement nach der Norm DIN EN ISO 13485:2016 stellt die Kontrolle der Entwicklung und Herstellung von Medizinprodukten, wie auch die systematische Überwachung (Surveillance) von Produktauffälligkeiten, und ihre behördliche Kontrolle (Vigilanz) sicher.
Im letzten Schritt der Konformitätsbewertung muss der Hersteller auf Basis gesetzlicher Produktanforderungen garantieren, dass das Produkt die technische und klinische Dokumentation nachweislich erfüllt und insbesondere die biologische Verträglichkeit gegeben ist. Diese genormte Biokompatibilitätsprüfung gemäß ISO 10993 stellt sicher, dass keiner der verwendeten Stoffe, wie beispielsweise biostatische Additive, den Patienten schadet. Auch endständige Sterilfilter müssen diese Prüfung bestehen, denn sie stehen, indirekt über das filtrierte Wasser, mit dem Patienten im Kontakt.
Erfüllt der Hersteller die beschriebenen Vorgaben der strengen gesetzlichen Auflagen, kann die Konformität ausgesprochen werden und das Produkt als CE-gekennzeichnetes Medizinprodukt zugelassen werden.
Die Anwendung für den Patienten, Anwender und Dritte kann als sicher angesehen werden. Der Hersteller wird von einer Behörde überwacht und steht gegenüber dem Anwender in einer breiten Verantwortung.
CE-gekennzeichnete Medizinprodukte zur Infektionsprävention sind aus diesem Grund sinnvoll, insbesondere in der derzeitigen pandemischen Situation.